電気陰性度と極性
電気陰性度
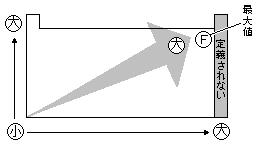
原子が原子間の共有電子対を引き寄せる強さの尺度を電気陰性度という。
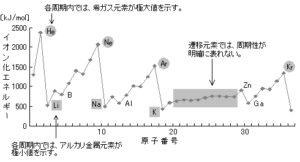
電気陰性度の値は、イオン化エネルギーと電子親和力の値から計算されたものであり、一般に、周期表の右上の元素ほど大きい。ただし、18族(希ガス)元素では定義されない。
分子の極性
極性分子
電気陰性度の異なる原子間の結合では、共有電子対は電気陰性度の強い原子側に引き寄せられるため、分子は部分的に正や負の電気を帯びた状態になる。このような状態の分子を極性分子という。
(例)NH3 , H2O , SO2
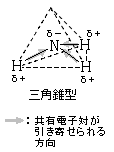
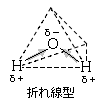
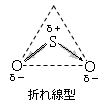
無極性分子
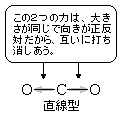
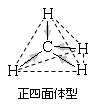
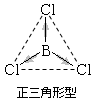
同種の原子からなる二原子分子や、分極していても分子の立体構造により分子全体の正の電荷と負の電荷の重心が一致する分子では、極性を生じない。これを無極性分子という。
(例)CO2 , CH4 , BCl3