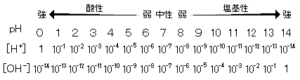
酸と塩基
酸・塩基の定義
アレニウスの定義
| 酸 | 塩基 |
| 水溶液中で電離してオキソニウムイオン*H3O+を生じる物質 | 水溶液中で電離して、水酸化物イオンOH-を生じる物質 |
| 〈例〉HCl+H2O ⇄ H3O++Cl- | 〈例〉Na OH ⇄ Na++OH- |
*一般にH+と略記して、水素イオンということが多い。
ブレンステッドの定義
| 酸 | 塩基 |
| 反応する相手に陽子H+を与える物質 | 反応する相手から陽子H+を受け取る物質 |
| 〈例〉HCl + H2O ⇄ H3O++Cl- (酸)HCl | NH3+ H2O ⇄ NH4++OH- (塩基)NH3 |
酸・塩基の価数
酸の価数…酸1分子が放出できるH+の数
塩基の価数…塩基1単位が放出できるOH-の数(受け取ることのできるH+の数)
| 価数 | 酸の例 | 塩基の例 |
| 1価 | 塩化水素HCl、硝酸HNO3、 酢酸CH3COOH | 水酸化ナトリウムNaOH、 水酸化カリウムKOH、 アンモニアNH3 |
| 2価 | 硫酸H2SO4、硫化水素H2S、 シュウ酸(COOH)2 | 水酸化カルシウムCa(OH)2、 水酸化バリウムBa(OH)2 |
| 3価 | リン酸H3PO4 | 水酸化鉄(Ⅲ)Fe(OH)3 |
【注】多価(価数が2価以上)の酸や塩基は、多段階に電離する。
〈例〉H3PO4 ⇄ H++H2PO4-
H2PO4- ⇄ H++HPO42-
HPO42- ⇄ H++PO43-
酸・塩基の強弱
水素イオン濃度
酸(HA)や塩基(BOH)などを水中に添加すると
HA → H+ + A-
BOH → B+ + OH-
のように一部が分かれる。このことを電離という。
さらに、電離のしやすさによって強いものと弱いものに分けられる。
強いものとは HCl→H++Cl- のように加えた量のほぼ100%が電離するものである。
弱いものとは CH3COOH⇄CH3COO-+H+ のように加えたものの2%以下くらいしか電離しないものである。
電離度α
電離している割合のことで、0<α≦1(α=1のときを完全電離という)
電離度α=$\displaystyle \frac{電離した電解質の物質量}{溶かした電解質の物質量}$
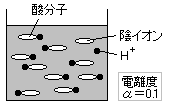
電離度の大小
αが大きいもの…強酸(強塩基)
αが小さいもの…弱酸(弱塩基)
| 強酸 | HCl、 H2SO4 、HNO3 | 強塩基 | 「かなりバカ」と覚える KOH、NaOH、LiOH、Ba(OH)2、Ca(OH)2 |
| 弱酸 | CH3COOH 、H2CO3 | 弱塩基 | NH3 、Cu(OH)2 、Al(OH)3 |