中和と塩
中和
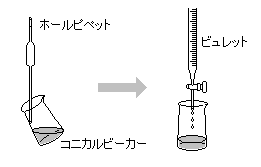
中和…酸と塩基が反応して、その性質を打ち消しあう変化。
酸と塩基が反応すると水と塩(えん)が出来る。
HCl + KOH → H2O + KCl
(酸) (塩基) (水) (塩)
塩の分類
正塩(完全に中和されたもの) Na2SO4 (CH3COO)2Ca
酸性塩(Hが残っているもの) NaHCO3 NaHSO4
塩基性塩(OHが残っているもの) Cu(NO3)OH MgCl(OH)
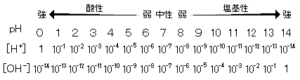
塩の液性
強酸+強塩基→中性
〈例〉KCl[HCl+KOH] Na2SO4[2NaOH+H2SO4]
強酸+弱塩基→酸性
〈例〉CuCl2[HCl+Cu(OH)2] NH4NO3[HNO3+NH3]
弱酸+強塩基→塩基性
〈例〉CH3COOK[CH3COOH+KOH]
弱酸+弱塩基→中性くらい
〈例〉(NH4)2CO3[H2CO3+2NH3]
特別に注意するべき塩(頻出)
NaHSO4…酸性
NaHCO3…塩基性
KF…塩基性