中和滴定
中和の量的関係
酸と塩基が中和しているとき、酸のH+と塩基のOH-は必ず等しくなる。そのため酸または塩基の濃度がわかれば、中和滴定により計算で、未知の塩基または酸の濃度を求めることができる。
基本的にはすべてaCV=bC’V’の式にしたがう。
aCV=bC’V’
a:酸の価数
b:塩基の価数
C、C’:モル濃度(酸または塩基)
V、V’:体積(酸または塩基)
滴定用実験器具
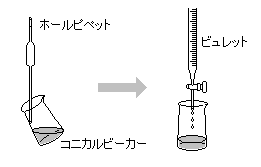
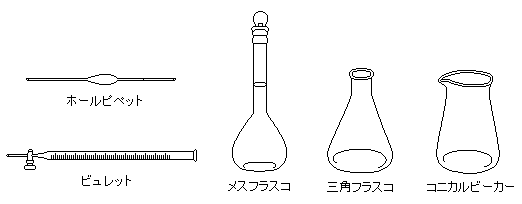
ホールピペット…一定体積の液体を正確にはかりとる。加熱乾燥不可。内壁をこれから使用する溶液で数回洗ってから使用する(共洗い)。
ビュレット…滴定液を入れ、滴下する。加熱乾燥不可。内壁を滴定液で数回洗ってから使用する。(共洗い)
覚え方『トで終わるのは共洗い』
メスフラスコ…はかりとった試料や試薬に溶媒を加え、一定の体積に希釈する。加熱乾燥不可。内壁を純水で洗い、ぬれたまま使用する。
受器…口が狭く、底が平らな受器を用いる(三角フラスコ、コニカルビーカー)。内壁を純水で洗い、ぬれたまま使用する。
滴定曲線
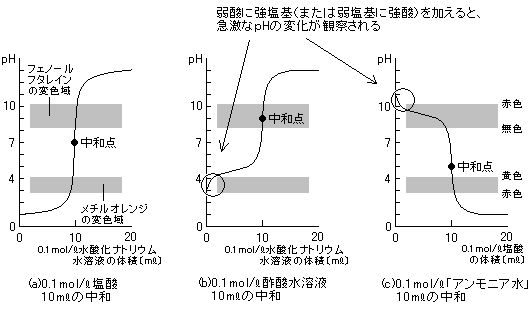
強酸―強塩基の滴定→指示薬…フェノールフタレイン・メチルオレンジ
弱酸―強塩基の滴定→指示薬…フェノールフタレイン
強酸―弱塩基の滴定→指示薬…メチルオレンジ
弱酸―弱塩基の滴定→滴定には適していない。

