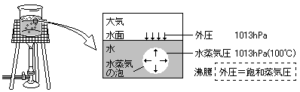
気体の法則と状態方程式
気体の法則
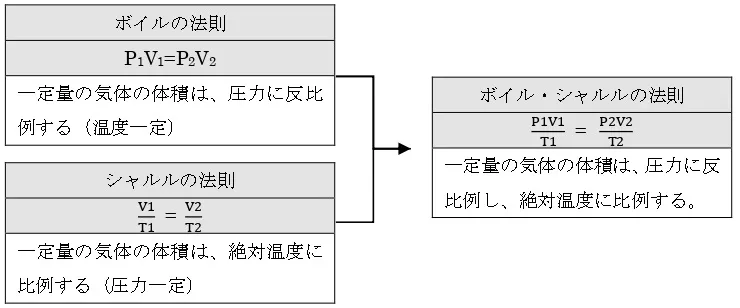
【注】温度は、通常セルシウス温度(単位℃)や絶対温度(単位K)が用いられる。これらの温度の間には、次の関係が成立する。
T〔K〕=t〔℃〕+273
-273℃は絶対温度の0Kに相当し、この0Kを絶対ゼロ度という。絶対ゼロ度では、物質のすべての運動が停止すると考えられる。
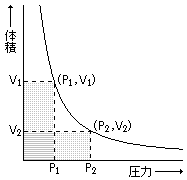
ボイルの法則:体積と圧力は反比例する
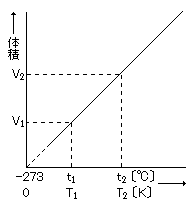
シャルルの法則:体積は絶対温度に比例する
気体の状態方程式
n〔mol〕の気体が、P〔Pa〕、T〔K〕のもとで、V〔ℓ〕を占めるとき、次の関係式が成立する。この式を気体の状態方程式という。
PV=nRT
R:気体定数…8.31×103〔Pa・ℓ/(K・mol)〕
または8.3〔J/(K・mol)〕
【注】圧力の単位がatmの場合は、R=0.082〔atm・ℓ/(K・mol)〕となる。
- 分子量と気体の状態方程式
PV= RT (w:質量 M:分子量) - 密度と気体の状態方程式
P= RT (d=:密度)
気体の分子量の求め方
| 標準状態における密度の利用 | M=密度×22.4 |
| 比重の利用 | M=既知分子量×分子量既知の気体に対する比重 |
| 気体の状態方程式の利用 | M= = |