分子と共有結合
構造式と電子式
共有結合に関与していない電子対を非共有電子対という。
〈考え方〉各電子には固有の価標(結合手)があり、余すことなく完全に結合させて作る。
| 原子 | H | C | N | O | Cl |
| 価標数(原子価) | 1 | 4 | 3 | 2 | 1 |
| 最外殻 電子数 | 1 | 4 | 5 | 6 | 7 |
- まず化学式を書く。
- 価標を使って構造式を書く。
- 価標1つに電子を2つ書く。
- 最外殻電子の数をあわせる。
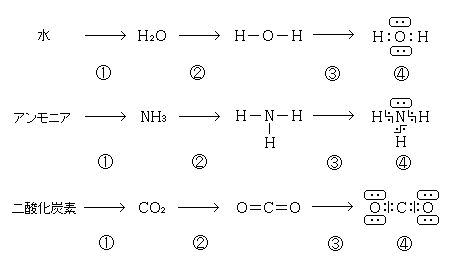
共有結合に関与していない電子対を非共有電子対という。
〈考え方〉各電子には固有の価標(結合手)があり、余すことなく完全に結合させて作る。
| 原子 | H | C | N | O | Cl |
| 価標数(原子価) | 1 | 4 | 3 | 2 | 1 |
| 最外殻 電子数 | 1 | 4 | 5 | 6 | 7 |
